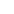政策园地
国家药品监督管理局药品审评中心发布关于公开征求《罕见疾病药物临床研发中应用去中心化临床试验的技术指导原则》意见的通知
2023年11月24日,为助力罕见疾病药物临床研发,落实“以患者为中心”的理念,指导科学、规范、可推广的DCT开展模式,国家药品监督管理局药品审评中心发布关于公开征求《罕见疾病药物临床研发中应用去中心化临床试验的技术指导原则》意见的通知。
阅读原文
链接:https://www.cde.org.cn/main/news/viewInfoCommon/9d0dead52438cd2e6c081a02022a8be1
分享到:
相关科室 |
相关医生 |
相关文章 |
相关咨询 |
相关视频 |
相关疾病
版权声明 隐私声明 联系我们 网站帮助 院长信箱 网站地图 友情链接
- 北京大学第一医院 版权所有
 北京市西城区西什库大街8号
北京市西城区西什库大街8号 100034
100034 83572211
83572211
京ICP备13027525号 京卫网审字(2001)27号 京公网安备 11040202430046号 工信部链接:https://beian.miit.gov.cn/